Jeanne Brugère-Picoux* et Jean-Luc Angot**
* Professeur honoraire de l’Ecole nationale vétérinaire d’Alfort, membre de l’Académie nationale de médecine, présidente honoraire de l’Académie vétérinaire de France
** Docteur vétérinaire, inspecteur général de santé publique vétérinaire au Conseil général de l’alimentation, de l’agriculture et des espaces ruraux (CGAAER), président de l’Académie vétérinaire de France
Article publié avec l’aimable autorisation de l’Académie vétérinaire de France.

Résumé – La majorité des maladies émergentes ou résurgentes qui ont été observées ces dernières décennies sont des zoonoses et celles-ci ont été parfois la cause de graves crises sanitaires, la pandémie due à la Covid-19 représentant une crise majeure qui ne connaît pas de précédent. Les facteurs favorisant l’émergence ou la résurgence d’une maladie sont très divers et parfois associés : agents pathogènes importés par des vecteurs (animaux de compagnie, oiseaux migrateurs, commerce international, etc.), modification de l’environnement (déforestation, travaux de terrassement, augmentation des zones éclairées, etc.), engouement pour de nombreuses espèces exotiques modifiant leurs écosystèmes en vue de leur commerce, voire de leur consommation, augmentation de la densité de la faune sauvage urbaine ou rurale, modification de nos relations avec l’animal (visites pédagogiques de fermes, nouveaux animaux de compagnie). L’important est de maintenir un écosystème favorable à tous, animaux sauvages ou domestiques et l’Homme. Il n’y a qu’une seule santé dans un seul monde où interviennent la médecine humaine, la médecine vétérinaire et l’environnement.
Il y aura toujours des maladies émergentes
Dans l’ouvrage Destin des maladies infectieuses, Charles Nicolle écrivait en 1933 : «Il y aura donc des maladies nouvelles. C’est un fait fatal. Un autre fait, aussi fatal, est que nous ne saurons jamais les dépister dès leur origine… Il faut aussi bien se résigner à l’ignorance des premiers cas évidents. Ils seront méconnus, confondus avec des maladies déjà existantes… Pour qu’on la reconnaisse plus vite, il faudrait que l’infection nouvelle soit d’importation exotique et douée d’un pouvoir marqué de contagiosité, telle autrefois la syphilis à son débarquement en Europe.» L’arrivée de la Covid-19 en Europe puis dans les Amériques démontre que la vision des maladies émergentes par cet illustre médecin microbiologiste, prix Nobel en 1928, est toujours d’actualité près de quatre-vingts années plus tard. La majorité des maladies émergentes ou résurgentes qui ont été observées en France ou dans le monde ces dernières décennies sont des zoonoses et celles-ci ont été parfois la cause de graves crises sanitaires (encéphalopathie spongiforme bovine, pandémie grippale due au virus H1N1, etc.), la pandémie due à la Covid-19 représentant une crise majeure qui ne connaît pas de précédent. Le commerce international croissant des animaux domestiques et sauvages (ou de denrées alimentaires d’origine animale), l’introduction accidentelle ou volontaire d’espèces animales dans des zones géographiques nouvelles, l’engouement pour de nombreuses espèces exotiques modifiant leurs écosystèmes en vue de leur commerce, voire de leur consommation, sont à l’origine de l’émergence ou de la résurgence de ces zoonoses.
Du fait de leur formation les confrontant aux maladies de plusieurs espèces animales, les vétérinaires ont des notions de pathologie comparée, de biosécurité et d’épidémiologie qui les aident souvent dans le diagnostic d’une nouvelle maladie émergente touchant une espèce. En raison de l’existence d’un réseau sanitaire vétérinaire permettant une surveillance des maladies émergentes, ils sont aussi rapidement disponibles pour limiter la propagation de celles-ci, aidés pour cela par un réseau de laboratoires vétérinaires départementaux très performants et par une industrie du médicament vétérinaire efficace. Leur action concerne aussi le contrôle sanitaire de notre alimentation. Ils ont toujours été des acteurs de terrain efficaces pour limiter la propagation des maladies comme ce fut le cas lors des grandes campagnes de prophylaxie contre des maladies redoutables pour l’élevage et la santé publique (tuberculose, brucellose, fièvre aphteuse…). Les vétérinaires sont en effet des acteurs à part entière de la santé publique du fait que près de 75% des maladies émergentes humaines sont des zoonoses. Entre 1940 et 2008, Jones et al. [1] ont identifié 335 maladies émergentes dans le monde, dont 60% étaient des zoonoses (parmi lesquelles 72% étaient dues à la faune sauvage), 54 % étaient dues à des bactéries ou des rickettsies, 23% étaient des maladies vectorielles. Nous limiterons ce document à certains exemples de maladies émergentes qui peuvent être dues à plusieurs facteurs associés ou non : importation et/ou dissémination d’agents pathogènes par de nouveaux vecteurs, émergence ou résurgence d’agents pathogènes, le plus souvent découverts lors d’une modification de l’environnement de leur réservoir tellurique ou d’un écosystème animal (déforestation, travaux de terrassement, notamment dans des zones tropicales où il existe une grande biodiversité animale, augmentation des zones éclairées liée à l’urbanisation et au développement des transports entraînant des changements d’habitats, consommation de certaines espèces animales sauvages), extension et augmentation de la densité de la faune sauvage urbaine (faune liminaire) ou rurale réservoir d’agents zoonotiques, modification de nos relations avec l’animal (visites pédagogiques de fermes, nouveaux animaux de compagnie).
Importation d’agents pathogènes
Les possibilités d’importation d’un nouvel agent pathogène sont variées. Ces importations peuvent être le fait d’un commerce ou de l’importation illégale d’animaux porteurs, du transport d’agents pathogènes par des oiseaux migrateurs (ou du transport par ces oiseaux de vecteurs comme la tique) ou par des vecteurs inanimés [2].
Importation d’animaux de compagnie porteurs
Certaines maladies émergentes peuvent survenir avec l’importation d’animaux dont le statut sanitaire est inconnu (porteurs ou réservoirs asymptomatiques, malades en cours d’incubation, non déparasités). Les exemples sont nombreux chez les animaux sauvages et/ou les animaux de compagnie importés : chiens enragés importés illégalement du Maroc, rats de Gambie importés aux Etats-Unis et porteurs du virus de la variole du singe, rats de compagnie infectés par le virus du cowpox, reptiles porteurs de salmonelles, etc.
Transport d’agents pathogènes par des oiseaux migrateurs
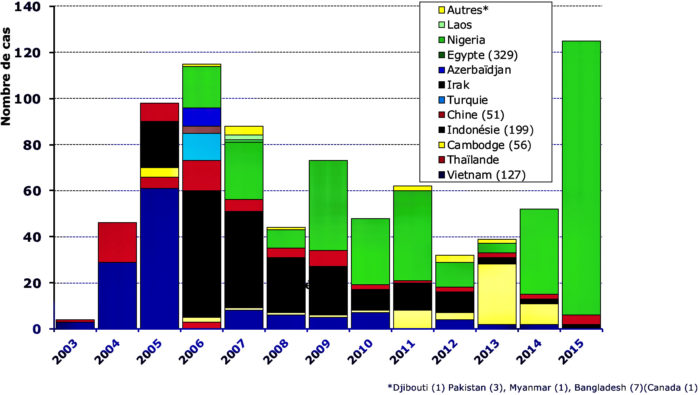
On connaît le risque lié à la contamination des volailles par le virus influenza aviaire hautement pathogène qui représente un véritable problème économique dans les pays touchés, d’où le nom de peste aviaire donné à cette maladie hautement contagieuse qui concerne principalement le domaine de la santé publique vétérinaire. En effet, on peut se tromper en annonçant à tort un risque de pandémie humaine comme ce fut le cas de la peste aviaire (dénommée «grippe aviaire») due à un virus influenza H5N1 hautement pathogène qui est apparu en Chine en 1996 et qui a envahi progressivement l’Asie puis le continent européen. Il faut dire qu’après l’épidémie de grippe espagnole due à un virus H1N1 en 1917 (40 à 100 millions de morts dans le monde), la grippe asiatique en 1957 due à un virus H2N2 (1 à 4 millions de morts), puis la grippe de Hong Kong due à un virus H3N2 (1 à 2 millions de morts), l’Organisation mondiale de la santé (OMS), attendant une nouvelle pandémie, pensa, comme d’autres épidémiologistes réputés, que le virus aviaire H5N1 pouvait être un bon candidat. C’était méconnaître la médecine vétérinaire, où la peste aviaire n’était pas classée dans les zoonoses avant l’épisode de Hong Kong de 1996 avec le virus H5N1. Ce virus a pu contaminer l’Homme lors de contacts très étroits avec des volailles vivantes en Asie mais il ne s’est jamais adapté à l’espèce humaine. De 2003 au 20 janvier 2020, il n’y a eu que 861 malades, dont 455 décès, sans transmission interhumaine, ce qui ne correspond pas à la définition d’une épidémie ! (fig. 1). Plus tard, en 2009, il y a eu une épidémie de grippe humaine A due à un virus H1N1 (dénommée à tort «grippe porcine») qui fit 500 000 morts dans le monde.
Transport de tiques par les oiseaux migrateurs
Les oiseaux migrateurs peuvent aussi favoriser le transport de vecteurs de maladies tels que les tiques. Ce type de transport est particulièrement suspecté dans la diffusion en Europe d’une tique redoutable, Hyalomma marginatum, vectrice potentielle de la fièvre hémorragique de Crimée-Congo (des cas mortels ont été signalés en Espagne et en Turquie) et de la fièvre boutonneuse due à Rickettsia aeschlimannii (observée en Allemagne) [3]. L’exemple de la «tique tueuse asiatique», Haemaphysalis longicornis, responsable d’une fièvre hémorragique pouvant s’accompagner d’un taux de mortalité de 50% chez les personnes âgées de plus de 60 ans et désormais présente sur le continent américain, démontre que ce danger est bien réel [4].
Transport de tiques par des vecteurs inanimés
Le cas particulier des transports d’agents pathogènes liés au commerce est bien connu avec la diffusion des moustiques tigres, notamment d’un continent à l’autre par des pneus, véritables réservoirs d’eau stagnante favorisant leur multiplication. Le trafic aérien a souvent été en cause pour expliquer certaines maladies exotiques importées en particulier dans l’environnement des aéroports (paludisme, fièvre jaune). Deux maladies émergentes récentes non zoonotiques, la fièvre catarrhale ovine ou FCO et la maladie de Schmallenberg, ayant touché des ruminants dans des zones qui n’étaient pas considérées à risque en Europe septentrionale il y a moins de deux décennies devraient faire prendre conscience des nouveaux risques de maladies émergentes. C’est à partir de la région de Maastricht, carrefour mondial du commerce des fleurs, que ces deux maladies caractérisées par des avortements et des malformations fœtales, ont diffusé de manière identique, la première en 2006, la seconde en 2011, touchant la Belgique, l’Allemagne, le Luxembourg, les Pays-Bas et la France. L’origine exotique des agents pathogènes isolés laisse fortement suspecter l’introduction d’un insecte infecté avec les fleurs puis la possibilité d’un relais avec un vecteur autochtone du genre Culicoïdes. Cependant, ces deux exemples remarquables à cinq années d’intervalle n’ont pas conduit à traiter préventivement les fleurs exotiques avec un insecticide ; ce type d’accident pourrait donc survenir à nouveau pour menacer d’autres espèces, dont l’espèce humaine ! Rappelons que la FCO fut la plus grande épizootie de ces trois dernières décennies et que l’on observe actuellement une recrudescence des arboviroses zoonotiques circulant en Europe (West Nile, virus Usutu, encéphalite à tiques…). On peut d’ailleurs noter l’émergence récente en France du virus Usutu [5] ou de l’encéphalite à tiques, transmise par une morsure de tique ou par l’ingestion d’un produit laitier contaminé. Les symptômes de cette encéphalite débutent par un syndrome grippal estival nécessitant actuellement un diagnostic différentiel avec la Covid-19 [6].
Importation d’origine inconnue du virus du Nil Occidental aux Etats-Unis en 1999 : rôle des animaux sentinelles lors d’une zoonose émergente
La fièvre du virus du Nil occidental ou VNO (West Nile), due à un Flavivirus, était connue depuis longtemps sur de nombreux continents. Les oiseaux sauvages en sont les réservoirs essentiels. Cette maladie a connu une émergence historique en 1999 dans un zoo du Bronx : la survenue d’une mortalité anormale chez des corneilles dans ce zoo fut d’abord considérée par le Centre de référence des maladies émergentes (Center for Disease Control ou CDC) d’Atlanta comme un «problème uniquement vétérinaire», le VNO n’étant pas connu dans cette zone géographique. Ce n’est que plus tard qu’une relation entre ce virus et des cas d’encéphalites chez l’Homme fut découverte. Depuis, la maladie a envahi les Etats-Unis, représentant maintenant la principale cause des encéphalites arbovirales humaines. Chez l’Homme, de 1999 à 2019, on a dénombré 2381 décès et plus de 25 000 formes neuro-invasives ont été observées [7]. Les circonstances de l’apparition du VNO aux Etats-Unis démontrent l’importance qu’il faut accorder aux «animaux sentinelles» qui, par un taux de mortalité anormale, peuvent annoncer une maladie émergente menaçant l’Homme. Rappelons aussi qu’une autre arbovirose zoonotique, la fièvre de la vallée du Rift, pourrait menacer l’Europe en raison de la présence probable du virus dans le Maghreb et en Turquie comme le montre l’observation de sérologies positives [8, 9]. Ce virus est actuellement particulièrement actif en Mauritanie.
Emergence ou résurgence d’agents pathogènes par modification d’un écosystème
Des agents pathogènes ont pu émerger lorsque leur environnement a été modifié. L’origine peut être tellurique mais, le plus souvent, il s’agit d’un changement dans l’écosystème de leur réservoir animal.
Maladies telluriques (résurgentes)
La fièvre charbonneuse est une maladie ancienne qui peut émerger à nouveau lorsque les spores de Bacillus anthracis, enfouies dans le sol pendant de nombreuses décennies (à l’époque où l’on enfouissait les cadavres des animaux), sont ramenées à la surface (du fait de travaux de terrassement, d’une montée de la nappe phréatique…) puis sont ingérées par des ruminants. Cela explique les cas sporadiques observés dans de nombreux pays, dont la France.
Maladies liées à une modification d’un écosystème animal
Bien souvent, on peut remarquer qu’une maladie émergente apparaît dans une contrée où l’on a favorisé la possibilité d’un contact plus étroit avec diverses espèces animales. Ces zones à haut risque, appelées «points chauds», où l’on peut observer l’émergence d’une nouvelle maladie humaine correspondent à la modification de l’écosystème d’une espèce sauvage ayant pu contaminer alors l’Homme. Les exemples sont nombreux ces dernières années, notamment avec les chauves-souris, tant en Asie avec le syndrome respiratoire aigu sévère (Sars), la Coronavirus disease 2019 ou Covid-19 et le virus Nipah qu’au Moyen-Orient avec le syndrome respiratoire du Moyen-Orient (Mers) ou en Afrique avec les fièvres hémorragiques comme l’Ebola ou la maladie de Marburg [10]. Ce n’est pas la biodiversité qui est en cause dans l’apparition de ces zoonoses mais plutôt la perturbation de l’écosystème de ces chauves-souris qui a favorisé l’émergence et la transmission d’un nouvel agent pathogène à l’Homme.
Coronavirus
Les coronavirus et plus spécifiquement des betacoronavirus, font partie des derniers virus responsables de zoonoses émergentes, comme le Sras et le Mers puis la Covid-19. Si l’origine zoonotique de ces maladies est connue avec pour réservoir les chauves-souris, les modalités de contamination le sont moins, notamment le rôle éventuel des hôtes intermédiaires suspectés. Le Sras (Sars en anglais) fut responsable d’une épidémie sévère de février à mai 2003 avec un taux de mortalité de 10%, tuant 774 personnes sur 8096 malades, surtout en Chine mais le Canada fut aussi très touché (avec 43 décès sur 251 malades). Il a fallu mettre en place d’importantes mesures de biosécurité pour stopper l’épidémie. Quand le Sras est arrivé à la mi-novembre 2002 dans la province du Guangdong, les cas n’ont pas été officiellement notifiés par crainte d’éventuelles retombées sociales ou économiques, permettant ainsi une large diffusion du virus. L’OMS n’a été prévenue que le 11 février 2003… Le Mers est apparu plus tard, en septembre 2012, et concerne principalement le Moyen-Orient, l’animal réservoir étant le dromadaire. A la fin de novembre 2019, 2494 cas ont été confirmés dont 858 décès (soit un taux de mortalité de 34,4%). L’Arabie Saoudite a été le pays le plus touché avec 2102 cas dont 780 décès, soit un taux de mortalité de 37,1%. Alors que les premiers cas de Sras ont été observés en 2002 dans la province du Guangdong, il s’est avéré que la source géographique du virus était dans la province de Yunnan, ou dans le sud-ouest de la Chine, le principal réservoir animal étant vraisemblablement des chauves-souris fer à cheval (Rhinolophus sinicus). Une surveillance a été effectuée pendant plus de cinq ans sur ces chauves-souris présentes dans une grotte de la province de Yunnan. Celle-ci a permis de démontrer l’importante quantité de coronavirus pouvant être hébergés par ces chiroptères, dont certains étaient proches du virus du Sras (Sars-CoV), d’où leur dénomination de Sars-related coronavirus (Sarsr-CoV). Ainsi, dès 2017, des scientifiques chinois du laboratoire de Wuhan soulignèrent l’importance de ces nouvelles informations sur l’origine et l’évolution du Sars- CoV et la nécessité de se préparer à l’émergence future de maladies comme le Sras. En 2019, cette même équipe chinoise indiquait qu’«il est très probable que les futures épidémies de coronaviroses comme le Sras ou le Mers proviendront de chauves-souris, et qu’il y a une probabilité accrue que cela se produise en Chine. Par conséquent, l’enquête sur les coronavirus de chauve-souris devient un problème urgent pour la détection des signes d’alerte précoce pour minimiser alors l’impact de ces futures épidémies en Chine.»… Il était surtout évident pour ces scientifiques que la Chine représentait la zone à haut risque (le point chaud) d’où partirait l’épidémie. La prédiction de ces scientifiques chinois s’est réalisée avec l’apparition en décembre 2019 d’une pneumonie d’origine inconnue touchant 59 personnes dans la ville chinoise de Wuhan. Les personnes atteintes avaient surtout fréquenté le marché de fruits de mer de la ville où d’autres animaux domestiques et sauvages étaient vendus, souvent vivants. Le 2 janvier 2020, ce marché fut immédiatement fermé sans que l’on ait recherché l’origine de la contamination parmi les espèces animales vendues. On sait maintenant que cette maladie émergente (Covid-19) est due à un coronavirus (Sars-CoV-2) où une autre chauve-souris fer à cheval (Rhinolophus affinis) est de nouveau incriminée en tant que réservoir. L’étude du génome du Sars-CoV-2 confirme qu’il s’agit d’un virus proche à 96,2% d’un coronavirus présent chez la chauve-souris (Sarsr-CoV;RaTG13), ce virus étant plus éloigné du virus du Sras (79%) ou de celui du Mers (50%). Cependant, on ne connaît toujours pas l’origine exacte de la contamination humaine par le Sars-CoV-2 alors qu’un lien épidémiologique avec un marché d’animaux vivants sauvages ou domestiques a été établi pour expliquer l’origine du Sras en Chine (certains animaux ont pu jouer le rôle d’hôte intermédiaire, notamment la civette palmiste masquée, Paguma larvata, d’origine sauvage ou provenant de fermes d’élevage vendues vivantes sur les marchés). Dans le cas du Sars-CoV-2, le pangolin (Manis pentadactyla et Manis javanica) est suspecté. Face à l’importante diffusion mondiale du Sars-CoV-2, le risque d’apparition d’un réservoir animal est souvent évoqué, notamment du fait d’une contamination animal-Homme qui a été observée dans des élevages de visons aux Pays-Bas mais aussi du fait de la contamination d’animaux de compagnie par leur propriétaire (Communiqué de l’Académie nationale de médecine et de l’Académie vétérinaire de France du 23 juillet 2020) [11].
Déforestation et virus Nipah
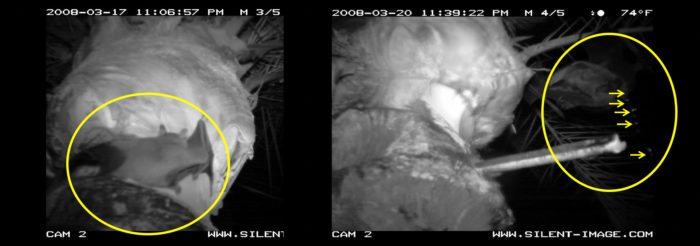
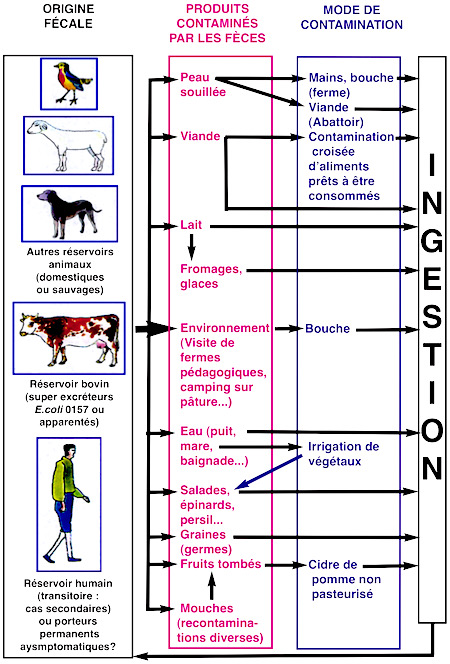
L’apparition d’encéphalites humaines dues au virus Nipah (Henipavirus, de la famille des Paramyxoviridae) en Malaisie et à Singapour représente un excellent exemple de maladie émergente pouvant s’implanter et diffuser du fait d’une déforestation. Celle-ci a provoqué, à partir de 1998, le déplacement de chauves-souris frugivores du genre Pteropus vers des fermes et des abattoirs favorisant un contact avec des porcs domestiques et l’Homme, provoquant une encéphalite souvent mortelle (taux de mortalité supérieur à 50%) [12]. Ce n’est que plus tard que l’on a découvert aussi la possibilité d’une origine alimentaire de cette affection redoutable, en particulier au Bangladesh entre fin 2004 et début 2005. La contamination se faisait par un jus de palme contaminé lui-même par l’urine de ces chauves-souris frugivores (fig 2 et 3, [13]).
Extension des «gîtes à tiques»
Au contraire, la réduction du nombre d’exploitants agricoles et le remplacement de certains champs par de la forêt ou des taillis, associés à une extension des zones périurbaines, ont été un facteur favorisant l’extension de certains vecteurs comme les tiques à l’origine de la maladie de Lyme, de l’ehrlichiose ou de l’encéphalite à tiques dans de nombreux pays. D’autres facteurs, notamment climatiques avec un hiver trop doux, mais aussi l’augmentation du nombre de cervidés ou de suidés, réservoirs sauvages facilitant la dissémination de ces vecteurs ont pu favoriser la multiplication des tiques voire leur progression dans certaines régions jusque-là indemnes. L’inquiétude liée à l’augmentation du risque de maladies vectorielles dues aux tiques n’est pas nouvelle. Par exemple, dès 2010, une plaquette de 26 pages informant sur les maladies transmises par les tiques (borréliose de Lyme, encéphalites à tiques, rickettsioses de type TIBOLA ou LAR, anaplasmose humaine, tularémie, fièvre Q), réunissant notamment médecins et vétérinaires, a été réalisée par le réseau Franche-Comté sous l’égide de l’Institut national de veille sanitaire et du ministère de la Santé.
Consommation d’animaux sauvages
L’exemple des marchés chinois mettant en contact des animaux sauvages vivants et l’Homme peut expliquer l’apparition du Sras et de la Covid-19, même si les hôtes intermédiaires ayant pu être un relais dans ces contaminations ne sont pas encore connus avec précision. Ce risque d’origine alimentaire est aussi connu en Afrique avec la consommation de la viande de brousse, notamment de singes, qui a pu favoriser une contamination par le virus du sida.
Augmentation de la faune sauvage urbaine ou rurale
Faune sauvage urbaine (rats, pigeons)
Bien que surnommés «rats volants», les pigeons représentent un risque moins important pour la santé publique [14] que les rats (réservoirs de leptospires, de salmonelles, etc.), dont on a pu observer une prolifération importante en région parisienne [15]. Parfois le risque peut être très important comme c’est le cas à Madagascar où les rats sont les réservoirs d’un bacille de la peste résistant aux antibiotiques [16]. Enfin, on peut aussi remarquer que les tiques responsables de maladies vectorielles en augmentation actuellement (cf. faune sauvage en milieu rural) peuvent être présentes dans les jardins privés ou publics en zone urbaine.
Faune sauvage rurale
Nous avons connu les modifications progressives de notre enseignement vétérinaire où, avant l’arrivée des automobiles, le cheval était l’animal le plus important puis, avec l’importance de la consommation de viande après la seconde guerre mondiale, l’enseignement des maladies des ruminants fut privilégié, notamment avec les grandes prophylaxies réalisées par les vétérinaires, destinées à limiter un risque zoonotique (comme la tuberculose et la brucellose) ou les pertes économiques dues à certaines affections non zoonotiques limitant les échanges commerciaux (fièvre aphteuse, par exemple). Cependant, malgré ces grandes prophylaxies, on observe toujours la persistance de ces agents pathogènes dans la faune sauvage qui ne bénéficie pas d’une vaccination ou d’une surveillance sanitaire (avec une éradication des animaux malades ou à risque).
Faune sauvage réservoir de maladies du bétail
Le risque d’apparition d’une affection non zoonotique où la faune sauvage représente un réservoir dangereux pour les élevages est permanent. Nous l’avons vu pour la peste aviaire qui peut être apportée par les oiseaux migrateurs mais il peut s’agir d’un risque pour les élevages de porcs comme le montre actuellement la progression de la peste porcine africaine, qui a touché des pays voisins de la France comme la Belgique et l’Allemagne. Les pays asiatiques sont aussi confrontés à des épidémies de peste porcine classique interdisant tout commerce pour les pays contaminés. D’autres maladies du bétail peuvent reconnaître un réservoir dans la faune sauvage comme la paratuberculose (dont l’origine zoonotique est controversée), la FCO, la maladie de Schmallenberg, etc. [17].
Faune sauvage réservoir de maladies zoonotiques
La faune sauvage peut importer des agents pathogènes (virus du Nil occidental, influenza aviaire, virus rabique, virus Nipah) mais en France, elle peut aussi assurer la persistance de la tuberculose, de la brucellose, de l’hépatite E et de certaines zoonoses parasitaires ou favoriser une augmentation du risque de maladies transmises par les tiques [18]. Malgré l’éradication efficace de la tuberculose en France, des foyers peuvent réapparaître sporadiquement du fait de réservoirs sauvages comme les cervidés, les sangliers et les blaireaux. Un autre exemple est celui la brucellose sévissant actuellement dans le massif du Bargy en Haute-Savoie. Après la découverte d’un cas de brucellose dans un élevage laitier du Grand Bornand en avril 2012 et la relation entre cette infection et la contamination de deux jeunes enfants ayant consommé une tomme blanche venant de cette ferme, il a été démontré que la faune sauvage, en l’occurrence les bouquetins présents dans le massif du Bargy, était à l’origine de ces contaminations. La Brucella des bouquetins aurait pour origine une souche bovine, à savoir le dernier cas de brucellose bovine signalé en 1999 dans la région, cette souche ayant circulé en s’amplifiant pendant plusieurs années dans la population des bouquetins. La décision d’abattre les bouquetins âgés de plus de 5 ans, contaminés dans une proportion de 56% en 2013, a concerné principalement les mâles, d’où un accès prématuré des jeunes au rut et leur contamination puisque la maladie se transmet principalement par la voie vénérienne. Le bouquetin est une espèce sauvage protégée mais il n’en a plus le comportement dans le massif du Bargy comme l’ont constaté les promeneurs dans ce massif et il ne s’agit pas d’une espèce en voie de disparition. Il est apparu qu’un abattage total, même s’il ne peut pas être de 100% au sein d’une population sauvage, a représenté la solution la plus réaliste, considérant le risque non négligeable pour la santé publique, en particulier dans la région de production du reblochon fermier au lait cru. Il faut remarquer que la brucellose peut aussi exceptionnellement concerner le domaine des animaux de compagnie comme le chien [19]. Le cas particulier du virus de l’hépatite E (famille des Hepeviridae) représente un problème émergent dans de nombreux pays. Il s’agit du seul virus causant une hépatite rencontrée chez l’Homme et les animaux. Les réservoirs asymptomatiques de ce virus sont le porc, le sanglier, le cerf, le lapin, la mangouste ou le rat. Cette zoonose peut être transmise par des produits tels que la viande ou le foie de sanglier, de cerf ou de porc consommés crus ou insuffisamment cuits (comme la figatelle corse, riche en foie de porc). Enfin, l’augmentation de densité de la faune sauvage s’accompagne aussi d’un risque accru de maladies parasitaires zoonotiques transmises par l’alimentation [20, 21].
Modifications de nos relations avec l’animal
L’évolution actuelle de nos modes de vie nous a amenés à vivre plus souvent en région urbaine qu’à la campagne. Alors que la profession vétérinaire était surtout formée pour intervenir en région rurale chez les animaux de production il y a plus de 50 ans, on a pu observer une désertification progressive du milieu rural (comme chez les médecins) au profit d’une médecine urbaine des animaux de compagnie, plus confortable et plus lucrative. Si les zoonoses liées au contact trop souvent étroit entre les animaux de compagnie classiques comme le chien et le chat sont loin d’être négligeables [22], l’arrivée des nouveaux animaux de compagnie favorise aussi celle de nouveaux agents pathogènes émergents.
Risque zoonotique lié aux nouveaux animaux de compagnie (NAC)
A part le lapin, les NAC ne sont pas toujours recommandés pour les enfants. Les petits rongeurs comme le hamster peuvent être porteurs de tularémie ou du virus de la chorioméningite lymphocytaire. Il faut aussi noter le nombre de plus en plus élevé de mustélidés (furets) comme animaux de compagnie [23] particulièrement sensibles au Sars-Cov-2.
Poxviroses et salmonelloses
Nous avons cité précédemment le risque de poxviroses résultant de l’importation de rats : le premier est l’épisode de l’importation de la variole du singe (Monkeypox) survenu dans les Etats du Midwest américain en 2003, avec plus de 70 cas humains identifiés (la source était des rats de Gambie, rongeurs importés d’Afrique vers les Etats-Unis pour être vendus comme animaux de compagnie et qui se sont avérés responsables, chez le vendeur, de l’infection de chiens de prairie, eux-mêmes vecteurs secondaires de la contamination humaine) ; le second exemple est européen : il s’agit de rats importés de Hongrie en tant que NAC (un dessin animé destiné aux enfants avait fait l’apologie de cet animal de compagnie) et qui étaient porteurs d’un autre orthopoxvirus, le cowpox. L’Allemagne a été le premier pays à lancer l’alerte à la fin des années deux mille avant que la France ne soit touchée. Il faut également souligner le risque réel, trop souvent sous-estimé, des salmonelloses transmises par les reptiles (plus de 90% sont porteurs asymptomatiques de salmonelles), dont la possession en tant que NAC devrait être déconseillée, en particulier en présence d’enfants, d’autant qu’aucun traitement ne permet l’élimination de l’agent pathogène. Ainsi, 3 à 5% des cas de salmonellose humaine aux Etats-Unis sont associés à un contact avec des NAC et le plus souvent, ce sont des reptiles. Ce risque a été également confirmé en France [24, 25].
Cas particulier d’une zoonose émergente due au virus Borna
La maladie de Borna (du nom de la ville de Borna en Allemagne) est connue depuis le XVIIe siècle chez les chevaux et les moutons. L’intérêt pour la maladie de Borna s’est accru en médecine vétérinaire à partir de 1993 suite à la découverte d’autres espèces sensibles (chat, autruche, bovins, chien…) et de son extension géographique (Etats-Unis, Suède, Israël, Japon…). Puis la découverte en 2015 d’un risque d’encéphalites mortelles dues à ce virus chez des propriétaires d’écureuils multicolores ou de Prévost en Allemagne (ces NAC n’étant pas autorisés en France), suivie par la confirmation en 2018 que ce virus pouvait provoquer d’autres cas d’encéphalites mortelles chez l’Homme, ont démontré le rôle zoonotique qui fut longtemps controversé de ce virus [26, 27].
Risque zoonotique lié aux visites de fermes pédagogiques et aux «petting zoos»
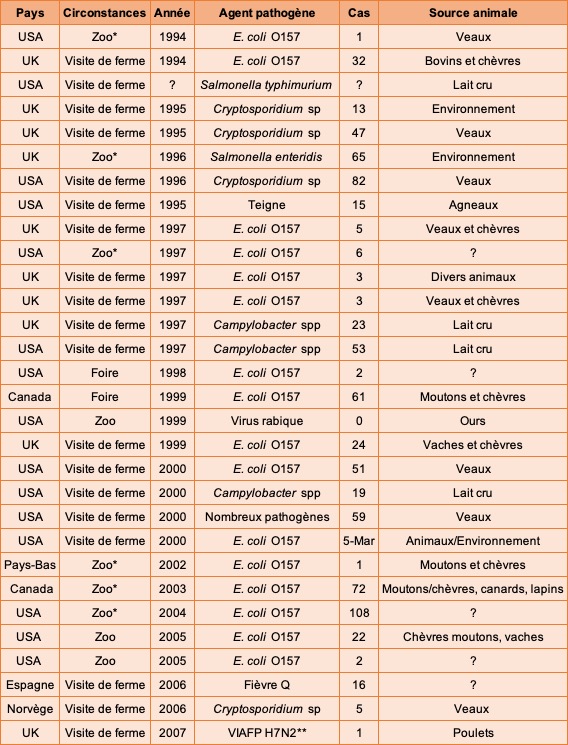
La mode des visites de fermes pédagogiques est relativement récente en France par comparaison avec les pays anglo-saxons. C’est peut-être la raison pour laquelle nous n’avons jamais connu les épisodes dramatiques rencontrés en Amérique du Nord ou au Royaume-Uni chez de très jeunes enfants contaminés par des colibacilles entérotoxinogènes provoquant un syndrome hémolytique et urémique (SHU) particulièrement grave (fig. 4, [28]). De même, relativement récemment, on a pu observer dans certains zoos des emplacements spécialement aménagés (appelés «petting zoos» par les Anglo-Saxons) pour permettre aux enfants d’être en contact étroit avec des animaux domestiques ou d’origine sauvage pour les caresser (chèvres, moutons, daims, etc.). Depuis quelques années, de nombreuses publications signalent l’importance croissante du risque de zoonose dans ces conditions et l’urgence à les prévenir par des mesures strictes de biosécurité vis-à-vis des agents suivants : Escherichia coli O157:H7, Salmonella, Coxiella burnetti, Mycobacterium tuberculosis, Campylobacter et les dermatophytes agents de teignes (cf. tableau 1). Face à ces risques émergents liés aux visites de fermes pédagogiques et aux «petting zoos», l’Académie vétérinaire de France a adopté un avis sur ce sujet le 6 novembre 2008.
* zones aménagées dans les zoos pour un contact étroit entre les enfants et des animaux de la ferme
** VIAFP H7N2 : virus influenza aviaire faiblement pathogène de sous-type H7N2
Médecine humaine, médecine vétérinaire et médecine environnementale : une seule santé
Ces exemples de maladies émergentes témoignent que nous ne serons jamais à l’abri de nouvelles maladies émergentes et que la faune sauvage est souvent impliquée du fait de l’action de l’Homme qui a perturbé leur écosystème, notamment par une modification de leur environnement ou leur chasse en vue de leur consommation. La mise en évidence, chez les Chiroptères, de coronavirus pouvant provoquer deux épidémies comme le Sras à partir de 2002 puis la Covid-19 en 2019 doit nous amener à reconsidérer nos stratégies de prévention de ces endémies en évitant le risque de contamination par une cohabitation trop étroite avec les chauves-souris par modification de leur écosystème et leur consommation. Les répercussions médicales, économiques et médiatiques de la pandémie due à la Covid-19 démontrent l’importance à accorder à l’étude des coronavirus chez les Chiroptères mais aussi à protéger ces espèces, dont certaines sont insectivores et fort utiles dans la lutte contre les insectes. Il faut aussi éviter les possibilités de transfert de certains virus émergents vers l’Homme par le mélange de plusieurs espèces d’animaux sauvages ou domestiques vendus le plus souvent vivants sur les marchés asiatiques, véritables chaudrons réservoirs de virus et centres d’amplification pour les infections émergentes. Il faut espérer que l’interdiction des marchés d’animaux vivants, et plus particulièrement d’animaux sauvages, sera maintenue avec rigueur en Chine. Cela impliquera une importante modification des habitudes alimentaires dans plusieurs régions chinoises. L’important est de maintenir un écosystème favorable à tous, animaux sauvages ou domestiques et l’Homme. Il n’y a qu’une seule santé dans un seul monde où interviennent la médecine humaine, la médecine vétérinaire et l’environnement. C’est pourquoi il est nécessaire de mettre en œuvre de manière opérationnelle le concept Une seule santé/One Health, à toutes les échelles. Ce concept transdisciplinaire doit être pris en considération dans la stratégie nationale pour la biodiversité, dans la stratégie de l’Union européenne en faveur de la biodiversité à l’horizon 2030 et au niveau des organisations internationales compétentes, y compris celles en charge de l’environnement et de la biodiversité, avec la création d’un Haut Conseil de la santé placé auprès du secrétariat général des Nations Unies.
[2] Brugère-Picoux J., Chomel B. Risques d’introduction et voies d’importation de maladies infectieuses exotiques en Europe par les animaux ou les produits d’origine animale. Bull Acad Natl Méd. 2009, 193 (8):1805-1818.
[3] Brugère-Picoux J. Installation de la tique Hyalomma marginatum en Europe du Nord. La Dépêche Vétérinaire. 2019, 1496:14.
[4] Beard C.B., Occi J., Bonilla D.L., Egizi A.M., Fonseca D.M., Mertins J.W. et al. Multistate Infestation with the Exotic Disease-Vector Tick Haemaphysalis longicornis – United States, August 2017-September 2018. MMWR. 2018, 67:1310-1313.
[5] Brugère-Picoux J. Une zoonose émergente due au virus Usutu. La Dépêche Vétérinaire. 2018; 1443:14.
[6] Communiqué de l’Académie nationale de médecine et de l’Académie vétérinaire de France du 12 juin 2020, Cet été, les syndromes pseudo-grippaux ne seront pas tous des Covid-19.
[7] Zientara S., Beck C., Lecollinet S.Arboviroses émergentes : fièvre West Nile, fièvre catarrhale ovine et virus Schmallenberg. Bull Acad Natl Med. 2020 Sep 28. doi: 10.1016/j. banm.2020.09.041.
[8] Gür S., Kale M., Erol N., Yapici O., Mamak N., Yavru S. The First Serological Evidence for Rift Valley Fever Infection in the Camel, Goitered Gazelle and Anatolian Water Buffaloes in Turkey. Trop Anim Health Prod. 2017, 49:1531-1535.
[9] EFSA. Rift Valley Fever – Epidemiological Update and Risk of Introduction into Europe. 20 janvier 2020.
[10] Brugère-Picoux J. Covid-19 : origine de la zoonose et modes de contamination. Droit Animal, Ethique et Sciences. 2020, 105.
[11] Brugère-Picoux J. Covid-19 : une étude montre une circulation significative du virus chez des chats et chiens dont le propriétaire était infecté. La Dépêche Vétérinaire. 2020, 1542:12.
[12] Vaillancourt J.P., Brugère-Picoux J. Le virus Nipah, un exemple d’agent pathogène émergent. In Risques d’importation et d’implantation en Europe des maladies infectieuses exotiques. Brugère-Picoux J., Rey M., éditeurs. Paris, Lavoisier, 2010, 71-87.
[13] Luby S.P., Rahman M., Hossain M.J., Blum L.S., Husain M.M., Gurley E. et al. Foodborne Transmission of Nipah Virus, Bangladesh. Emerg Infect Dis. 2006, 12:1888-1894.
[14] Brugère-Picoux J. Pigeons. Quel risque pour notre santé ? Revue du Palais de la découverte. 2010, 368:34-43.
[15] Brugère-Picoux J. Rats en milieu urbain : des risques zoonotiques réels. La Dépêche Vétérinaire. 2018, 1435:12.
[16] Cabanel N., Bouchier C., Rajerison M., Carniel E. Plasmid-Mediated Doxycycline Resistance in a Yersinia pestis Strain Isolated from a Rat. Int J of Antimicrobial Agents. 2018 51(7):249-254.
[17] Brugère-Picoux J., Vaissaire J. Rôle de la faune sauvage dans la transmission aux animaux de rente des maladies non réglementées. Séance commune avec l’Académie vétérinaire de France, 2011.
[18] Brugère-Picoux J., Le Floc’h Soye Y. Importance de l’implication de la faune sauvage dans les zoonoses émergentes ou résurgentes. Bull Acad Natle Méd. 2014, 198:1411-1422.
[19] Fontbonne A. L’identification récente d’un cas de brucellose canine en élevage canin impose de ne pas l’oublier. 2020.
[20] Thompson R.C.A., Kutz S.J., Smith A. Parasite Zoonoses and Wildlife: Emerging Issues. Int J Environ Res Public Health. 2009, 6:678-693.
[21] Dupouy-Camet J., Yera H., Bourée P., Aliouat-Denis C.M. Zoonoses parasitaires d’origine alimentaire à réservoir sauvage en France : aspects en santé publique. Epidémiol et santé anim. 2017, 71:25-34.
[22] Chomel B., Sun B. Zoonosis in the bedroom. Emerg Infect Dis. 2011, 17(2):167-172.
[23] Fédération vétérinaire européenne, 2018.
[24] Colomb-Cotinat M., Le Hello S., Rosières X., Lailler R., Weill F.X., Jourdan-Da Silva N. Salmonelloses chez des jeunes enfants et exposition aux reptiles domestiques : investigation en France métropolitaine en 2012. Bull Epidémiol Hebd. 2014, 1-2.
[25] Angot M., Labbe F., Duquesnoy A., Le Roux P. Co-infection rotavirus-Salmonella lié aux tortues : à propos de deux cas de zoonoses domestiques. Archives de Pédiatrie. 2017, 24:747-748.
[26] Brugère-Picoux J. Ecureuil multicolore et écureuil de Prévost : risque zoonotique lié au bornavirus VSBV-1. La Dépêche Vétérinaire. 2017, 1383:11.
[27] Brugère-Picoux J. Maladie de Borna des chevaux et du mouton : une zoonose émergente provoquant des encéphalites mortelles en Allemagne. La Dépêche Vétérinaire. 2020, 1513:12.
[28] Brugère-Picoux J. Le risque de zoonose inhérent aux visites de fermes pédagogiques. Bull Soc Vét Prat de France. 2010, 94:25-33.

